Rezistence bakterií vůči antibiotikům má kořeny u ježků dávno před nástupem farmaceutického průmyslu
Objev penicilinu odstartoval novou éru v léčbě bakteriálních infekcí. I přes to lékaři od té doby narážejí na bakterie, které jsou vůči antibiotikům rezistentní. Někteří odborníci nahlas mluví o nadužívání antibiotik a jejich slábnoucím účinku. Jak ale ukazuje výzkum mezinárodního vědeckého týmu, jehož součástí je i docent Pavel Hulva z naší katedry biologie a ekologie Přírodovědecké fakulty Ostravské univerzity, tato rezistence má kořeny ve zvířecí říši dávno před objevem Alexandra Fleminga i spuštěním hromadné výroby antibiotik. Své závěry teď publikovali v prestižním časopise Nature.
Antibiotika nám na nejrůznější neduhy způsobené bakteriálními infekcemi předepisují lékaři téměř 80 let. Málokdo si dnes ale uvědomuje, že jde prapůvodně o přírodní látky a jakési „chemické zbraně“, které houby od nepaměti používají na obranu vůči bakteriím. O příčinách rezistence vedou lékaři i vědci dlouhodobě debatu. Mezinárodní vědecký tým, jehož součástí byl i docent Pavel Hulva z naší katedry biologie a ekologie, teď hledal odpovědi přímo v přírodě – konkrétně u ježků. Na povrchu jejich těla žijí mikroskopické houby trichofytóza, které produkují beta-laktamová antibiotika, jež je chrání vůči bakteriím.
Tento objev však nebyl jednoduchý, předcházela mu rozsáhlá aktivita mezinárodního týmu, zajišťující vzorkování stěrů z kůže ježků po celé Evropě, sekvenování genomů stafylokoků, biogeografickou analýzu získaných dat, biochemické analýzy antibiotik i mikrobiologické testování rezistence jednotlivých kmenů.
Jak dokazuje studie, kterou vědecký tým publikoval v prestižním časopise Nature, právě u těchto hub je možné jasně najít kořeny vzniku stafylokoků rezistentních na methicilin (označovaných zkratkou MRSA – methicilin-resistant Staphylococcus aureus). To vše navíc dávno předtím, než se antibiotika naplno začala využívat v lidské a veterinární medicíně.
Jde tak o další důkaz přínosu moderních technologií a přístupů (genomika aj.), které umožňují mnohem komplexnější pohled na živou přírodu než dosud. Díky nim se ukazuje, že v přírodě je vše propojeno – těla živých organismů jsou jakýmisi vnitřními ekosystémy, složenými z celé řady menších tvorů (virů, bakterií, prvoků, hub i bezobratlých), označovaných novým pojmem holobiont (nahlas se mluví například o zdravotním významu kilogramů bakterií, které žijí ve střevě člověka), jež jsou zase provázány s vnějším ekosystémem (životním prostředím).
Již zmíněná studie v časopise Nature zdůrazňuje právě tuto provázanost a koncept „jednoho zdraví“. Čili skutečnost, že zdraví lidí, zvířat i ekosystémů spolu souvisí a je třeba vše vzájemně propojovat – jak přístupy lidské medicíny, veterinárního lékařství tak ochrany přírody. Pro příklady nemusíme chodit navíc daleko. V poslední době se nahlas hovoří o příkladech zvířecí nákaz přenosných na člověka (tzv. zoonózy), které často souvisejí s ničením životního prostředí. Například přenos eboly na lidi z populace kaloňů souvisí dle všeho s rozsáhlým kácením pralesů v Africe, přenos koronavirové nákazy (jako např SARS a COVID-19) je pak dle všeho zapříčiněn destrukcí ekosystémů a konzumací divokých zvířat v přelidněné Asii. Také u ježků, které vědecký tým využil pro svou studii platí, že se dostali do blízkosti lidí v Evropě poté, co byla zničena polootevřená parkovitá krajina tvarovaná velkými kopytníky a šelmami, o jejíž oživení se ochranáři v současnosti opětovně snaží.

Jak jste se k tématu ježků a rezistence na antibiotika dostal?
Ježkům jsme se s mojí bývalou studentkou Barborou Černou Bolfíkovou (mimochodem Ostravskou rodačkou) začali věnovat v roce 2006. Ježci patří ke středně velkým hmyzožravcům s pomalým metabolismem a hibernací, jejich rozšíření a mikroevoluce byla proto výrazně ovlivněna oscilacemi klimatu během pleistocénu. Ježci západní a východní navíc vytvářejí ve střední Evropě kontaktní zónu. Tyto druhy jsou proto vhodným modelem pro fylogeografický a speciační výzkum, na který se naše pracovní skupina zaměřila. Od roku 2012 jsme o ježcích publikovali řadu prací, většinou zaměřených na molekulární ekologii a fylogeografii, ale i na evoluci fenotypu nebo parazitů. Původním zaměřením jsem molekulární biolog, v magisterském stupni jsem studoval adaptivní mutagenezi u mikroorganismů, téma mikrobiomu a jeho evoluce mě proto zajímá.
Jaká byla vaše role při vzniku studie?
Vzhledem k dominantnímu postavení, které máme ve výzkumu ježků, jsem byl v roce 2017 osloven Jesperem Larsenem, prvním autorem studie, se žádostí o spolupráci na ježčím mikrobiomu. Protože mě koncept holobionta zajímá (nakonec mitochondriální DNA, kterou často zkoumáme, je pozůstatek původního endosymbionta, mikrosatelity jsou často parazitické elementy DNA a máme i řadu parazitologických prací), rád jsem souhlasil. Oslovil jsem Barboru, společně jsme se s Jesperem v Kodani setkali a od té doby řešili různé aspekty studie. Pak jsme se účastnili sběru vzorků. Analýzy genomů probíhaly v Kodani. První verze rukopisu zahrnovala asi dvacet autorů s dominancí veterinárních specialistů. Snažil jsem se do článku vnést evoluční a ekologický pohled, což se nakonec doufám podařilo. Je pozitivní, že takové to klasické výkladové schéma o „zlém“ patogenu a jeho „nevinné“ oběti se v éře biologie velkých dat posouvá k poněkud holističtějšímu pojetí, který přeci jen více odpovídá realitě.
Ježků se tedy nemusíme bát?
Určitě se jich nemusíme bát. Většina infekčních onemocnění, která kolují v lidské populaci, byla na lidi přenesena ze zvířat v minulosti a v současnosti k přenosu ze zvířat dochází v měřítkách celé planety a dlouhých časových období. Pravděpodobnost přenosu nemoci z myši, ježka nebo netopýra žijících na vaší zahrádce se při dodržování běžných hygienických standardů západní společnosti blíží nule.
Odkazy:
- https://doi.org/10.1038/s41586-021-04265-w (online)
- https://www.nature.com/articles/s41586-021-04265-w.pdf (PDF)
- https://rdcu.be/cEpmu (Sharedit)
Česká a zahraniční média:
- https://ct24.ceskatelevize.cz/veda/3424290-odolne-bakterie-se-na-cloveka-prenesly-z-jezku-jeste-pred-rozsirenim-antibiotik-ukazal
- https://www.bbc.com/news/science-environment-59883336
- https://www.nytimes.com/2022/01/05/science/hedgehog-mrsa-drug-resistant-bacteria.html
- https://www.thetimes.co.uk/article/superbug-mrsa-may-have-evolved-in-hedgehogs-about-200-years-ago-szxqkqs9x
- https://www.telegraph.co.uk/news/2022/01/05/mrsa-superbug-emerged-hedgehogs-200-years-ago-study-finds/
- https://www.newscientist.com/article/2303390-a-type-of-mrsa-evolved-in-hedgehogs-long-before-the-first-antibiotics/
1) Stafylokok rezistentní na methicilin (MRSA) byl přítomen u ježků zhruba od roku 1800 (od nástupu průmyslové revoluce), dlouho předtím než v roce 1959 přišel na trh methicilin. 
Foto: Petra Hulvová
2) Petriho miska s agarem, na kterém roste houba (F) produkující antibiotikum. Na levé polovině misky rostou bakterie rezistentní na antibiotikum (MRSA), na pravé polovině misky jsou citlivé bakterie (MSSA) – antibiotikum produkované houbou je zabíjí a vytváří čistý půlkruh vpravo uprostřed. 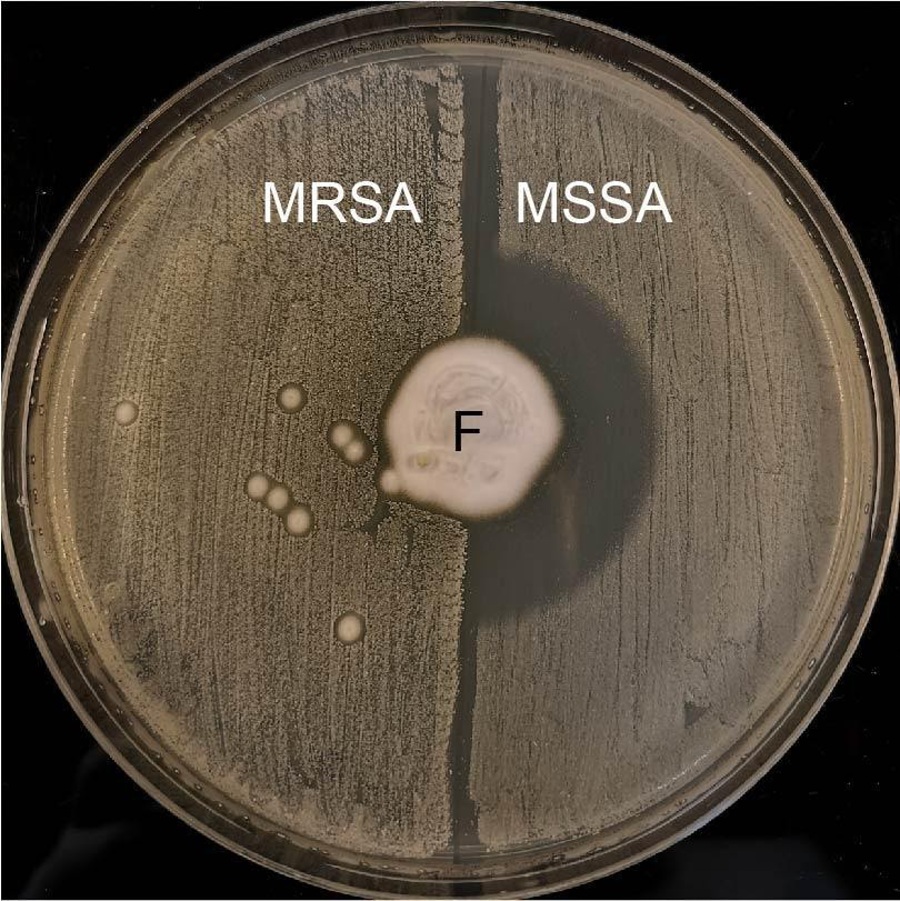
Foto: Claire L. Raisen
3) Houba žijící na těle ježků může produkovaným antibiotikem zabít bakterie citlivé na methicilin, zatímco rezistentní kmeny se dokáží ubránit. 
Ilustrace: Adam Sejer
4) Koncept jednoho zdraví: zdraví člověka, zvířat a ekosystémů spolu souvisí a aktivity lidské medicíny, veterinárního lékařství a ochrany přírody od sebe nelze oddělit. 
https://www.biomedcentral.com/collections/OneHealth
Citace: Larsen J. et al. (2022) Emergence of methicillin resistance predates the clinical use of antibiotics. Nature.
Zveřejněno / aktualizováno: 10. 01. 2022























